微针——在药物递送和POC诊断方面具有巨大潜力的微型装置

微针有可能在药物输送和诊断方面彻底改变医疗保健行业。这些微针小到肉眼无法看到,设计用于通过皮肤输送药物而不会引起疼痛。与注射或口服药物等传统方法相比,微针提供了一系列优点。它们具有微创性,甚至可以用于通过皮肤检测具有临床意义的物质。这篇博客文章将深入研究微针的世界,探索它们的潜力、好处、应用和挑战,以及它们如何准备彻底改变药物递送和诊断。
简介
微针是非常微小的微型针,长度通常在50至900µm之间。它们最初是在1976年提出的一种无痛和无创的药物递送方法 (1). 基于微针的器件是使用微制造技术制造的,由阵列中的尖锐突起组成。虽然最早的版本是由硅、金属或玻璃制成的,但最近的模型是由可生物降解和水凝胶基聚合物制成的。1998年,佐治亚理工学院的Mark Prausnitz指出,微针适合通过穿透人体皮肤的最上层进行透皮给药 (2).
微针类型
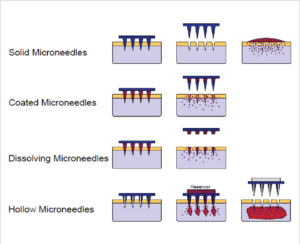
目前市场上有多种类型的微针。图 1 展示了针对不同应用开发的不同设计的微针。
固体微针 通过穿透皮肤发挥作用。这些微针一旦被拔出,就会留下微孔,可通过透皮贴片将药物涂抹在这些微孔中。
涂层微针 可将药物直接涂抹在针头阵列上,而无需使用贴片或涂抹器。一旦被体液水化,药物就会释放到皮肤中。
溶解性微针 含有可生物降解聚合物中的药物,可溶解在皮肤内部。
空心微针 具有储液器,可通过扩散或压力输送药物。
水凝胶形成的微针 包含一个药物储存器和一种膨胀材料,后者通过吸收膨胀基质中的间隙液来扩散药物。
微针应用
微针有多种用途,例如
药物和疫苗输送
用于糖尿病管理的胰岛素输送
胰岛素给药用于糖尿病管理是一项被广泛研究的应用 (3). 传统的每天多次注射的方法可能是痛苦和不方便的。另一方面,微针可以为胰岛素给药提供一种无痛且可能更有效的替代方案。
疫苗接种计划
微针也正在被研究用于输送疫苗 (4). 微针可将疫苗直接输送到富含免疫力的皮肤层,从而增强免疫反应。此外,微针的易用性和无痛性也使其成为大规模疫苗接种计划的一个极具吸引力的选择。
局部麻醉
微针已成功用于局部麻醉 (5)。微针可将麻醉剂直接注射到所需部位,提供快速有效的麻痹,而不会产生传统针头所带来的疼痛。 (5).
微针(化妆品)
微针也正在被研究用于疫苗的递送 (6). 2006 年,德斯蒙德-费尔南德斯博士(Dr. Desmond Fernandes)开发的第一台微针设备上市 (7),该设备成为现代的 Dermaroller。该设备的主要用途是利用固体微针更好地渗透护肤品,如促进胶原蛋白生成的精华素,帮助消除疤痕。
生物传感和医疗点诊断
微针可用于对皮肤中存的间质液或生物标记物进行微创采样。这些生物标记物可用于诊断目的,如监测用于糖尿病管理的葡萄糖水平或检测其他分析物。
微针的优点
从患者和治疗的角度来看,使用微针都有许多好处。
减轻疼痛和不适
对于需要频繁注射但又害怕打针的患者来说,微针是一种极佳的选择。微针非常细小,可以穿透皮肤而不会造成任何疼痛。研究表明,与传统皮下注射针相比,微针可将疼痛感降低 90% (8).
增加药物吸收
微针可穿透皮肤外层屏障,直接将药物输送到真皮层。真皮层血管丰富,能更快更有效地吸收药物。此外,通过微针给药避免了第一次通过代谢,这会降低某些药物的有效性。
副作用更小
微针贴片递送方法针对皮肤的免疫系统,以较低的疫苗剂量产生更强的免疫反应。这导致更有效地使用抗原 (9).
简单、独立的自我治疗
传统的皮下注射针头可能会导致意外的针头伤害、多次使用的污染风险和故意滥用,与此不同,廉价的一次性贴片形式的微针装置有可能在没有临床专业知识的情况下安全使用。
微针给药面临的挑战和未来发展方向
尽管微针取得了重大进展,但在被广泛采用之前,仍有一些挑战需要克服。
安全和监管问题
首先,需要解决安全和监管问题。虽然人们普遍认为微针是安全的,但还需要不断进行研究,以评估其长期安全性,特别是长期使用时的安全性。此外,还需要制定明确的监管准则,以确保微针产品的质量和安全。
可扩展性和成本效益
另一个挑战在于微针生产的可扩展性和成本效益。目前的生产工艺可能既复杂又昂贵,这可能会限制其广泛应用。目前正在努力开发可扩展且具有成本效益的制造方法,如光刻和3D打印(10),以克服这一挑战。
微针的稳定性和精确涂层
为确保微针的有效性,微针必须在整个储存、处理和应用过程中保持机械稳定性。在微针上涂抹药物、疫苗或其他生物制剂对保持微针的功能至关重要,但也会带来一些问题,如碳水化合物和聚合物加热,可能导致药物在高温下成型时分解 (11). 此外,微针的精确涂层和治疗物质的输送控制也是一项挑战。研究人员正在努力提高治疗物质的稳定性,优化微针本身 (12), 以及提高微针涂层的精确性和均匀性。
SCIENION微量喷点技术在微针涂层中的应用
微针涂层的方法多种多样,包括浸涂、滚涂或刷涂、喷涂和静电涂层(13).
Tyndall National Institute的最新研究 (14) 将 SCIENION 的微量喷点技术作为一种快速、精确和有效的微针涂层方法进行了研究。该方法在微针表面涂抹配方时表现出了极高的精确度。此外,考虑到可扩展性、生产速度和成本效益等因素,压电喷墨系统在大规模生产方面前景广阔。
结论
微针有可能彻底改变药物递送和诊断领域,提供一种无痛、高效的皮肤给药方法。微针具有减轻疼痛、增加药物吸收和提高病人依从性等优点,因此有望成为传统注射方法的替代品。目前的研发工作主要集中在解决与微针技术相关的挑战上,如安全问题、成本效益和稳定性。随着喷墨涂层等技术的不断进步,微针有可能改变我们提供药物的方式,为个性化医疗和改善患者预后开辟新的可能性。
参考文献
(1) Gerstel, M. S., & Place, V. A. (1976). Drug Delivery Device. Google Patents. US Patent No. US3964482A.
(2) Mark Prausnitz | School of Chemical and Biomolecular Engineering (gatech.edu)
(3) Jana, B. A., & Wadhwani, A. D. (2019). Microneedle – Future prospect for efficient drug delivery in diabetes management. Indian journal of pharmacology, 51(1), 4–10. https://doi.org/10.4103/ijp.IJP_16_18
(4) Sheng, T., Luo, B., Zhang, W., Ge, X., Yu, J., Zhang, Y., & Gu, Z. (2021). Microneedle-Mediated Vaccination: Innovation and Translation. Advanced drug delivery reviews, 179, 113919. https://doi.org/10.1016/j.addr.2021.113919
(5) Lee, B. M., Lee, C., Lahiji, S. F., Jung, U. W., Chung, G., & Jung, H. (2020). Dissolving Microneedles for Rapid and Painless Local Anesthesia. Pharmaceutics, 12(4), 366. https://doi.org/10.3390/pharmaceutics12040366
(6) Doddaballapur S. (2009). Microneedling with dermaroller. Journal of cutaneous and aesthetic surgery, 2(2), 110–111. https://doi.org/10.4103/0974-2077.58529
(7) Fernandes, D. (2005). Minimally invasive percutaneous collagen induction. Oral and Maxillofacial Surgery Clinics, 17(1), 51-63.
(8) Gill, H. S., Denson, D. D., Burris, B. A., & Prausnitz, M. R. (2008). Effect of microneedle design on pain in human volunteers. The Clinical journal of pain, 24(7), 585–594. https://doi.org/10.1097/AJP.0b013e31816778f9
(9) Vrdoljak A. Review of recent literature on microneedle vaccine delivery technologies. Vaccine: Development and Therapy. 2013;3:47-55
https://doi.org/10.2147/VDT.S34682
(10) Gülçür, M., Romano, J. M., Penchev, P., Gough, T., Brown, E., Dimov, S., & Whiteside, B. (2021). A cost-effective process chain for thermoplastic microneedle manufacture combining laser micro-machining and micro-injection moulding. CIRP Journal of Manufacturing Science and Technology, 32, 311-321.
(11) Donnelly, R. F., Morrow, D. I., Singh, T. R., Migalska, K., McCarron, P. A., O’Mahony, C., & Woolfson, A. D. (2009). Processing difficulties and instability of carbohydrate microneedle arrays. Drug development and industrial pharmacy, 35(10), 1242–1254. https://doi.org/10.1080/03639040902882280
(12) Lee, J. W., Park, J. H., & Prausnitz, M. R. (2008). Dissolving microneedles for transdermal drug delivery. Biomaterials, 29(13), 2113–2124. https://doi.org/10.1016/j.biomaterials.2007.12.048
(13) Ingrole, R. S. J., & Gill, H. S. (2019). Microneedle Coating Methods: A Review with a Perspective. The Journal of pharmacology and experimental therapeutics, 370(3), 555–569. https://doi.org/10.1124/jpet.119.258707
(14) O’Mahony, C., Hilliard, L., Kosch, T., Bocchino, A., Sulas, E., Kenthao, A., … & Bared, G. (2017). Accuracy and feasibility of piezoelectric inkjet coating technology for applications in microneedle-based transdermal delivery. Microelectronic Engineering, 172, 19-25.
(15) Rad, Z. F., Prewett, P. D., & Davies, G. J. (2021). An overview of microneedle applications, materials, and fabrication methods. Beilstein Journal of Nanotechnology, 12(1), 1034-1046.
Turner, J. G., White, L. R., Estrela, P., & Leese, H. S. (2021). Hydrogel‐forming microneedles: current advancements and future trends. Macromolecular Bioscience, 21(2), 2000307.